Capacidade térmica ou capacidade calorifica é a relação entre calor e temperatura em um corpo. Ou seja, ela é uma constante de proporcionalidade entre o calor Q recebido ou cedido pelo objeto e a variação Δt de temperatura do objeto.
A seguir, veja como calcular a capacidade térmica e como utilizá-la nos exercícios de física.
Capacidade térmica: o que é?
Quando dois corpos absorvem quantidades iguais de calor, a variação de temperatura que cada um sofre é, em geral, diferente uma da outra. Essa relação origina o conceito de capacidade calorifica de um corpo.
Se um corpo cede ou absorve uma quantidade de calor Q e sua temperatura sofre uma variação Δt, a capacidade calorifica desse corpo é, por definição, dada por: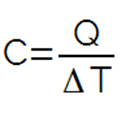 No SI, as unidades de capacidade calorifica são Joule por Kelvin [J/K] ou Joule por grau Celsius [J/°C].
No SI, as unidades de capacidade calorifica são Joule por Kelvin [J/K] ou Joule por grau Celsius [J/°C].
A palavra “capacidade” pode fazer com que você se confunda, pois sugere a seguinte analogia: um balde possui a capacidade de conter uma certa quantidade de água. Porém, isso é falso! Você não pode pensar que um objeto “contém” calor ou possui uma capacidade limitada de absorver calor.
É possível transferir uma quantidade ilimitada de calor para um objeto, contanto que uma diferença de temperatura seja mantida. É claro também que no meio desse processo de mudança de temperatura o objeto troque de estado físico: derreta ou evapore no processo.
Diferença entre capacidade térmica e calor específico
Não confunda capacidade térmica com calor específico. Essa confusão pode ocorrer pelo fato de ambos serem expressos pela letra c, porém, a capacidade térmica é representada pelo C maiúsculo, enquanto que o calor específico é expresso pelo c minúsculo.
A capacidade calorifica é equivalente ao calor específico para corpos, ao invés de substâncias. Ou seja, utilizamos o conceito de capacidade calorifica para tratar de substâncias como metais, madeiras, entre outras. Enquanto isso, a capacidade térmica é usada para tratar de calor em corpos.
É exatamente por isso que a capacidade calorifica é uma grandeza menos usada que o calor especifico. O calor específico é uma grandeza universal, ou seja, nas mesmas condições de pressão e temperatura, o calor especifico da água é o mesmo em qualquer lugar que ela esteja. Porém, de modo contrário, a capacidade calorifica de um corpo só vale para ele mesmo.
Relação entre capacidade térmica e calor específico
Podemos também escrever a capacidade térmica pelo calor específico. Sabemos que o calor Q pode ser escrito como: Q = c.m. Δt.
Com isso, podemos substituir o Q na fórmula da capacidade térmica pela expressão acima.
Teremos, então: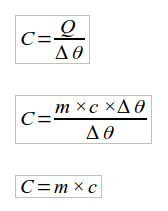 Sendo m o valor da massa do objeto.
Sendo m o valor da massa do objeto.
Com isso, temos, enfim, a relação entre as duas grandezas. Nesse caso, a unidade de medida da capacidade térmica C será cal/°C.
Exercícios Resolvidos
1) Um calorímetro sofre uma variação de temperatura de 20°C quando absorve uma quantidade de calor de 100 J.
A) Qual a capacidade calorifica?
B) Qual a quantidade de calor necessária para elevar a temperatura desse calorímetro em 50°C?
A) Aplicando a definição de capacidade calorifica, temos:
C = Q/ Δt
C = 100/20 = 7 J/°C
B) Da mesma forma:
Q = C. Δt
Q = 5 . 50 = 250 J.

